Chemický vzorecAdrenalon hydrochlorid(odkaz:http://www.bloomtechz.com/synthetic-chemical/api-researching-only/adrenalone-hydrochloride-cas-62-13-5.html) je C9H13NO3·HCl, CAS 62-13-5 a relativní molekulová hmotnost je 227,67. Je to bílý krystal nebo krystalický prášek. Tento prášek je obvykle bez zápachu a rozpustný ve vodě. Má dobrou rozpustnost ve vodě. Za normální teploty a tlaku se může rychle rozpustit a vytvořit bezbarvý a průhledný roztok. Roztok je kyselý. Jeho kyselost lze vyjádřit hodnotou pH. Jeho roztok má obvykle pH v rozmezí 2.5-4.5. Může se účastnit různých chemických reakcí, jako jsou esterifikační reakce, oxidační reakce a elektrofilní substituční reakce. Tyto reakce lze použít k syntéze derivátů se specifickými farmakologickými aktivitami.
Adrenalon hydrochlorid je elektrofilní a může se účastnit různých chemických reakcí. Níže je uvedeno několik typických reakcí:
1- Oxidační reakce: Adrenalon hydrochlorid může být oxidován na odpovídající ketonové deriváty silnými oxidanty, jako je peroxid vodíku (H2O2) nebo manganistan draselný (KMnO4), a tyto reakce se obvykle provádějí za kyselých podmínek. Následují obecné kroky oxidační reakce hydrochloridu adrenalonu:
A. Výběr silných oxidačních činidel:
Běžně používanými oxidanty jsou peroxid vodíku a manganistan draselný. Podle experimentálních podmínek a požadavků na reakci vyberte vhodný oxidant.
b. Reakční podmínky a reakční poměr reaktantů:
Za správných podmínek roztoku se adrenalon hydrochlorid a oxidant mísí v určitém reakčním poměru. Obecně se lepších výsledků dosáhne provedením reakce za kyselých podmínek.
C. Reakční teplota a reakční doba:
Řízení reakční teploty a reakční doby je klíčem k dosažení dobré oxidační reakce. Podle specifických experimentálních požadavků a vlastností reaktantů zvolte vhodnou reakční teplotu a reakční dobu.
d. Pozorování reakcí a sběr produktů:
Pozorujte jevy, jako je uvolňování plynu a změna barvy během reakce. Podle potřeb mohou být vybrány vhodné metody pro sběr a extrakci vytvořených oxidačních produktů.

2- Redukční reakce: Adrenalon hydrochlorid lze redukovat na odpovídající alkoholový derivát redukční reakcí. Redukční reakce obvykle používá redukční činidlo, jako je hydrogensiřičitan sodný (NaHSO3) nebo sulfoxid (DMSO).
A. Hydrogensiřičitan sodný (NaHSO3) redukce:
Běžným způsobem redukce hydrochloridu adrenalonu je použití hydrogensiřičitanu sodného (NaHS03). Chemická rovnice reakce je následující:
C9H12ClNO3plus NaHSO3plus H2O → C9H11NE3plus NaCl plus H2TAK4
Mezi nimi adrenalon hydrochlorid prochází redukční reakcí za vzniku Adrenalonu a vytváří chlorid sodný (NaCl) a kyselinu sírovou (H2SO4). V této reakci působí hydrogensiřičitan sodný jako redukční činidlo pro redukci hydroxylových skupin hydrochloridu adrenalonu na alkoholy. Tato reakce se provádí za kyselých podmínek.
b. Snížení sulfoxidu (DMSO):
Dalším běžně používaným redukčním činidlem je sulfoxid (DMSO). Níže je uvedena zjednodušená reakční rovnice pro redukci hydrochloridu adrenalonu sulfoxidem:
C9H12ClNO3plus C18H28O3S plus H2O → C9H11NE3plus C2H6OS plus HCl
Výsledkem této reakce je tvorba Adrenalonu, dimethylsulfoxidu (DMSO2) a kyselina chlorovodíková (HCl). Sulfoxid v této reakci redukuje hydrochlorid adrenalonu a redukuje jeho hydroxylovou skupinu na alkohol.
3- Esterifikační reakce: Hydroxylová skupina Adrenalon hydrochloridu může reagovat s anhydridem kyseliny nebo esterem kyseliny za vzniku odpovídajícího esterového derivátu.
4- N-alkylační reakce: Atom vodíku na aminovém dusíku Adrenalon hydrochloridu může reagovat s alkylhalogenidy za vzniku odpovídajících N-alkylových derivátů.
5- Ammonolýza: Adrenalon hydrochlorid je sloučenina adrenalinu s hydroxylovými a amidovými skupinami ve své molekulární struktuře. Reakce amonolýzy se týká chemické reakce s použitím amoniaku (NH3) nebo deriváty amoniaku pro konverzi amidové skupiny ve sloučenině na odpovídající aminovou skupinu.
Chemický vzorec hydrochloridu adrenalonu je C9H13NO3·HCl. Obsahuje amidovou skupinu (RCONH) a hydroxylovou skupinu (OH). Níže je uveden strukturní vzorec hydrochloridu adrenalonu:
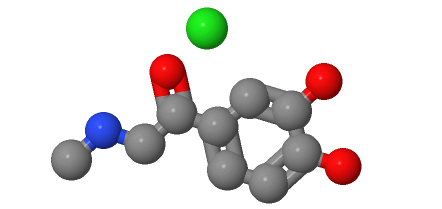
K provedení amonolýzy musíme přidat čpavek nebo čpavkovou vodu (NH4OH) jako zdroj amoniaku za alkalických podmínek. Za alkalických podmínek se amidová skupina (NHCONH2) bude hydrolyzován za vzniku odpovídající aminové sloučeniny. Níže je uveden zjednodušený chemický vzorec pro amonolýzu adrenalon hydrochloridu:
C9H12ClNO3plus NH4OH → C9H11NE3plus NH2CONH2plus HCl
Při této reakci reaguje hydrochlorid adrenalonu s čpavkem nebo čpavkovou vodou za vzniku adrenalonu, močoviny (NH2CONH2) a kyselina chlorovodíková (HCl). Toto je hydrolytická reakce, ve které je amidová skupina nahrazena atomem amoniaku, což vede k odpovídající aminové sloučenině.
Adrenalon hydrochlorid je sloučenina obsahující fenolické hydroxylové a amidové skupiny. Má některé specifické reakční vlastnosti, včetně kyselosti a zásaditosti, redoxní a nukleofilní substituce atd. Reakční vlastnosti Adrenalon hydrochloridu budou popsány níže.
1. Kyselost: Adrenalon hydrochlorid je hydrochlorid, který může v roztoku vytvářet kyselé prostředí. Může reagovat s alkálií za vzniku odpovídající soli a vody. Například reakce s amoniakem (NH3) poskytuje Adrenalon, chlorid amonný a vodu:
C9H12ClNO3plus NH3 → C9H11NE3plus NH4Cl
2. Oxidačně-redukční vlastnosti: Adrenalon hydrochlorid má fenolické hydroxylové skupiny, takže se může účastnit oxidačně-redukčních reakcí. Může být oxidován pomocí oxidačních činidel na odpovídající ketonové sloučeniny. Například, Adrenalon hydrochlorid může být oxidován kyslíkem na Adrenalon keton za alkalických podmínek:
2 C9H12ClNO3plus O2 → 2 C9H11NE3plus 2 HCl plus H2O
3. Nukleofilní substituce: Jelikož adrenalon hydrochlorid obsahuje amidové skupiny, má vlastnosti nukleofilní substituční reakce. Amidové skupiny mohou být substituovány nukleofily, jako je amoniak, aminy atd. za vzniku odpovídajících produktů. Například amonolýzu lze provést pomocí amoniaku (NH4OH) pro převedení amidových skupin na aminové skupiny:
C9H12ClNO3plus NH4OH → C9H11NE3plus NH2CONH2plus HCl
Toto je hydrolytická reakce, při které je amidová skupina nahrazena atomem amoniaku, což vede k odpovídající aminové sloučenině a kyselině chlorovodíkové.
4. Další reakce: Adrenalon hydrochlorid se může účastnit i jiných typů chemických reakcí, jako jsou esterifikační reakce, alkylační reakce atd. Je však třeba poznamenat, že esterifikace a alkylační reakce nejsou běžnými reakcemi Adrenalon hydrochloridu, protože nedochází k vhodné funkční skupiny ve své struktuře, aby se těchto reakcí přímo účastnily.

